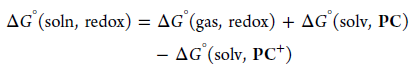这是本文档旧的修订版!
如何计算溶液中氧化还原Gibbs自由能变化
气体分子的Gibbs自由能计算请参考费米维基:气相分子的频率、红外IR、零点能、转动能量、转动惯量、熵、焓、热容与Gibbs自由能,液相自由能与焓的计算。本文讲解如何计算溶液中的氧化还原Gibbs自由能变化。依据的参考文献:
DFT as a Powerful Predictive Tool in Photoredox Catalysis: Redox Potentials and Mechanistic Analysis, Organometallics 2015, 34, 4218−4228
文献中(公式1),溶液中氧化还原Gibbs自由能变化分为三个部分的贡献:
第一项:氧化还原自由能变化,也就是离子化势(ionization potential);
第二项:还原产物PC的溶剂化后的Gibbs自由能;
第三项:氧化产物PC+的溶剂化后的Gibbs自由能。
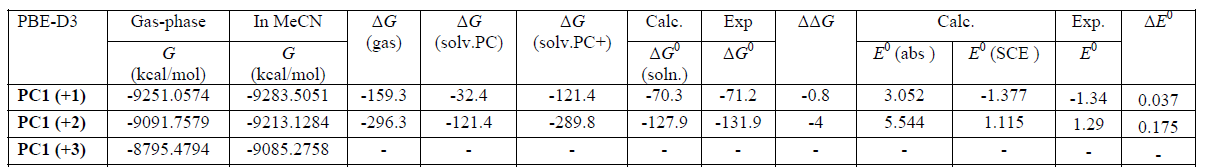
我们以该文的Supporting Information的Table S1中PC1(+2)为例,说明$PC1^{2+}$的这三个部分数值如何计算。下文中,PC1(2+)是文献中的表示方法,即PC12+,PC1(3+)即PC13+。
表S1:
准备公式中所需各项数据
1,计算$PC1^{2+}$的气相Gibbs自由能
也即表S1中的Gas-phase。计算前需要优化气相结构,计算方法参考费米维基:气相分子的频率、红外IR、零点能、转动能量、转动惯量、熵、焓、热容与Gibbs自由能,液相自由能与焓的计算即可。
结果应与文献中数值略有差别,文献中为-9091.7579kcal/mol
2,类似地计算$PC1^{2+}$在MeCN溶液中的Gibbs自由能
与上一步计算的区别仅仅在于多了model > Salvation的溶剂化设置,当然也需要在设置溶剂化的前提下,进行结构优化。类似地得到Gibbs free energy。
3,$PC1^{3+}$的气相Gibbs自由能以及在MeCN溶液中的Gibbs自由能
依照上述类似的方法,分别计算$PC1^{2+}$去掉一个电子之后,$PC1^{3+}$的气相Gibbs自由能以及在MeCN溶液中的Gibbs自由能(均需先做结构优化)。
溶液中氧化还原Gibbs自由能变化分
1,计算公式1中第一项
$PC1^{2+}$的△G0(gas,redox),也即表S1中的ΔG(gas)(采用文献中的数值):
ΔG(gas)
=$PC1^{2+}$的气相Gibbs自由能-$PC1^{3+}$的气相Gibbs自由能
=-9091.7579-(-8795.4794)
=-296.3 kcal/mol
2,计算公式1中第二项
$PC1^{2+}$的△G0(solv,PC),也就是表S1中的ΔG(solv.PC):
ΔG(solv.PC)
=$PC1^{2+}$在MeCN溶液中的Gibbs自由能-$PC1^{2+}$气相的Gibbs自由能(采用文献中的数值)
=-9213.1284-(-9091.7579)
= -121.3705 kcal/mol
3,计算公式1中第三项
$PC^{2+}$的△G0(solv,PC+),也就是表S1中的ΔG(solv.$PC^+$)一列,在这里$PC1^{2+}$的正离子,就是$PC1^{3+}$了,所以:
ΔG(solv.PC+)
=$PC1^{3+}$在MeCN溶液中的Gibbs自由能-$PC1^{3+}$气相的Gibbs自由能
-9085.2758-(-8795.4795)
=-289.8 kcal/mol
4,计算$PC1^{2+}$在MeCN溶液中氧化还原Gibbs自由能变化
△G0(soln,redox)
=ΔG(gas)+ΔG(solv.PC)-ΔG(solv.PC$^+$)
=-296.3+(-121.4)-(-289.8)
=-127.9 kcal/mol